
Рис. 2.5.4.1. Степени окисления атомов углерода
2.5.4. Реакции окисления алканов
В органической химии реакции окисления и восстановления рассматриваются как реакции, связанные с потерей и приобретением органическим соединением атомов водорода и кислорода. Эти процессы, естественно, сопровождаются изменением степеней окисления атомов.
Окисление органического вещества – введение в его состав кислорода и (или) отщепление водорода. Восстановление – обратный процесс (введение водорода и отщепление кислорода). Учитывая состав алканов (СnH2n+2), можно сделать вывод о их неспособности вступать в реакции восстановления, но возможности участвовать в реакциях окисления.
Алканы – соединения с низкими степенями окисления углерода (рис. 2.5.4.1) и в зависимости от условий реакции они могут окисляться с образованием различных соединений.

При обычной температуре алканы не вступают в реакции даже с сильными окислителями (Н2Cr2O7, KMnO4 и т.п.). При внесении в открытое пламя алканы горят. При этом в избытке кислорода происходит их полное окисление до СО2, где углерод имеет высшую степень окисления +4, и воды. Горение углеводородов приводит к разрыву всех связей С–С и С–Н и сопровождается выделением большого количества тепла (экзотермическая реакция).
Примеры:
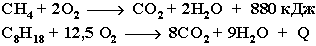
Процесс горения углеводородов широко используется для получения энергии (в двигателях внутреннего сгорания, в тепловых электростанциях и т.п.).
Уравнение реакции горения алканов в общем виде:

Из этого уравнения следует, что с увеличением числа углеродных
атомов (n) в алкане увеличивается количество кислорода, необходимого для
его полного окисления. При горении высших алканов (n >>1)
кислорода, содержащегося в воздухе, может оказаться недостаточно для их полного
окисления до СО2. Тогда образуются продукты частичного
окисления:
угарный газ СО (степень окисления
углерода +2),
сажа (мелкодисперсный углерод,
нулевая степень окисления). Поэтому высшие алканы горят на воздухе коптящим
пламенем, а выделяющийся попутно токсичный угарный газ (без запаха и цвета)
представляет опасность для человека.
Горение метана при недостатке кислорода происходит по уравнениям:

Последняя реакция используется в промышленности для получения сажи из природного газа, содержащего 80-97% метана. Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов. Например, при неполном окислении бутана (разрыв связи С2–С3) получают уксусную кислоту:

Высшие алканы (n>25) под действием кислорода воздуха в жидкой фазе в присутствии солей марганца превращаются в смесь карбоновых кислот со средней длиной цепи С12–С18, которые используются для получения моющих средств и поверхностно-активных веществ.
Важное значение имеет реакция взаимодействия метана с водяным паром, в результате которой образуется смесь оксида углерода (II) с водородом – "синтез-газ":

Эта реакция используется для получения водорода. Синтез-газ служит сырьем для получения различных углеводородов.